不明な症状の原因を突き止め、患者の未来を照らす
横浜市立大学大学院医学研究科遺伝学教室 教授 松本 直通先生
2021.8.6(聞き手:ステラ・メディックス 星 良孝)
なぜ症状を認めるのかが分からない患者に出会うことも少なくないかもしれない。かつては原因を突き止める手段が限られていたが、今は遺伝子検査の発達で状況が大きく変わった。
10年以上にわたり解析に取り組む横浜市立大学教授の松本直通先生に先端の動向を聞く。

横浜市立大学教授の松本 直通先生(撮影:村田 和聡、以下同)
毎日の診療の中で、症状/疾患の原因が分からない患者さんに遭遇する経験は誰しもあるでしょう。正常とは明らかに異なる症状/疾患を診たときに単に分からないままで終わるのではなく、直接、遺伝子解析の拠点に連絡するのは賢明だと思います」と松本先生は話す。
そうした場合に力を発揮するのが網羅的遺伝子解析となる。松本先生によると解析にかかるコストが低下し、一般的な診療の中で原因が分からないようなときでも相談できる機会は拡がっているという。
遺伝性疾患は9300種以上存在し、このうち約6100疾患は原因となる遺伝子が明らかとなっている。疾患特有の症状が現れていればよいが、思いもよらない症状を呈する疾患が遺伝子異常で起きている可能性もある。通常の診療のほか、新生児マススクリーニングのような検診による先天代謝異常症の幅広い拾い上げも行われている。しかし、それでも様々な機会をすり抜けて未診断のままになっているケースはある。
「診療科によらず、遺伝的な背景のある病気に少なからず出会うことがあります。一つ一つはまれであったとしても、その種類は多く、集合体として見ると頻度は少なくありません」と松本先生は語る。
未診断症例を診断し、希少疾患の原因遺伝子を特定する体制の進化
日本は難病克服のための研究を推進する体制がここ10年で大きく進化した。
横浜市立大学遺伝学教室では国の予算を得て難病の網羅的遺伝子解析拠点を2011年から開設、原因不明の様々な難病症例に対する網羅的遺伝子研究を積極的に行ってきた。これまでの総解析数は1万6000検体を超えた。
「解析によってすべての症例の原因となる遺伝子変異の特定には至っていないものの、原因不明の症状を呈する患者さんに遺伝子解析を行うと、およそ3人に1人は原因遺伝子変異の特定が可能となっている。全く新しい疾患を見いだすこともあり、2011年以来、新たに原因遺伝子を特定した疾患は65疾患になった」と松本先生は話す。
図・横浜市立大学における希少疾患の原因解明率(出典:横浜市立大学)
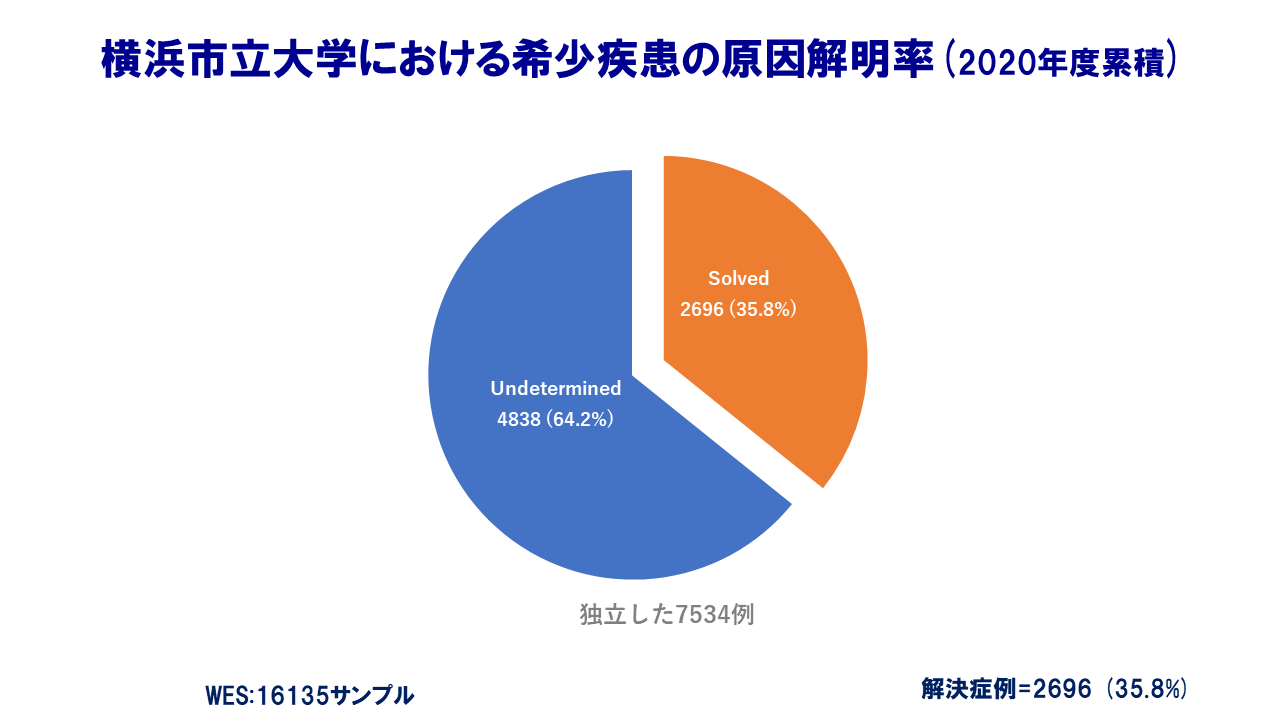
横浜市立大学の網羅的遺伝解析の対象になった希少疾患7534例のうち2696例(オレンジ部分)の原因が解明された。
松本先生らのように、現在、全国に「希少難治性疾患に関する全ゲノム医療推進に資する研究拠点」が8カ所存在しており、希少疾患の原因遺伝子の究明を進めている。「私たちの解析拠点では、神経疾患や骨関連の疾患の解析が得意であるように、それぞれの拠点が得意な分野を持ちながら精力的に解析研究を進めている」と松本先生は説明する。
さらに、2015年からは、日本医療研究開発機構(AMED)により、診断がつかない症例を体系的に診断するプロジェクト「未診断疾患イニシアチブ(Initiative on Rare and Undiagnosed Diseases : IRUD、アイラド)」が始まっている。
当初は小児と成人に分かれたグループからスタートし、成人のグループは国立精神・神経医療研究センター、小児のグループは国立成育医療研究センターが取りまとめ機関となった。現在は小児・成人の区別はなくなり統合され国立精神・神経医療研究センターが取りまとめ機関である。横浜市立大学はIRUD発足当時から小児・成人両方のIRUD解析センターを務めるほか、IRUD拠点病院にもなり現在に至る。
「不明の症状のある患者さんの原因を調べようとしたときに、問い合わせをする医療機関の選択肢が増えたのはよかったです。私は、世界的にも最も早い時期から難病の網羅的遺伝子解析に関する論文を発表していたこともあり、さまざまな症例が全国から送られていました。現在では各難病の遺伝子解析拠点がそれぞれ活発に活動し、拠点間でもコラボレーションを行うことは珍しくありません。未診断の疾患に、既知疾患の遺伝子異常が見つかることがあり、遺伝子解析をやるまで気付けないことも少なくなく、医療側も遺伝子解析の威力を認識するようになってきています。今後はこの遺伝子解析の機会をいかに増やすかが重要だろうと考えています」と松本先生は述べる。

横浜市立大学教授の松本 直通先生
原因を特定することで劇的に改善するケースがある
原因が分かることで治療につながり、症状の劇的な改善に導くことができることがある。
松本先生は、「2015年には、遺伝子解析によって、ドーパミンやセロトニンの生成ができなくなる芳香族Lアミノ酸脱炭素酵素(AADC)欠損症という劣性遺伝病を遺伝子解析で特定できたケースがありました。この症例を含む6例で、自治医科大学で進められるアデノ随伴ウイルスベクターを用いた遺伝子治療の効果が発表されています」と振り返る。
2018年には、原因が不明のまま寝たきりだったロシアの10代少女の遺伝子解析を行い、葉酸代謝に関わる受容体の欠乏を招く遺伝性疾患を特定した。葉酸誘導体の処方が治療になると分かり、症状は劇的改善を見せた。
横浜市立大学の症例ではないが、東北大学の研究チームが原因不明の目と脳の腫瘍性疾患に対して遺伝子解析を行い、がん遺伝子の一つであるBRAFの変異を確認し、抗がん剤として既に承認されているBRAF阻害薬による治療に結びつけた事例もある。この症例では治療により腫瘍の大幅に縮小が報告された。
松本先生は、「英国のジェノミクスイングランドという研究においては、遺伝子検査で遺伝子変異が特定されたものをアクショナブルとしています。直接に薬の処方につながらなくとも、診断を届けること自体がアクショナブルであると見なしています。原因解明までの追加検査目的で様々な病院を探すこと(診断オデッセイ)を不要にするからです。治療によって症状を改善できる疾患もありますが、遅れると治療効果が低くなる場合もあります。そのためにも早期に原因を特定して、治療・改善に結びつけることが望ましい」と話す。
見つける技術が向上している
遺伝子検査の技術も進んでいる。松本先生は、「格段に分かる情報が増えている。一口に遺伝子解析といっても進化している。常に効果的で、強力な解析法を模索している」と説明する。
ゲノムは約30億塩基から成り立っているが、初期の次世代シーケンサーでは100塩基ほどの短い塩基配列を細切れに読む仕組みになっていた。そのために同じ塩基配列の繰り返し(リピート配列)の伸長のような場所の状態を正しく読み取ることができなかった。松本先生は、ロングリードシーケンスと呼ばれる、1万塩基~2万塩基という長い塩基配列を一気に読む技術を用いて従来にない詳細な情報の分析を進めている。DNAを構成する四塩基のうち、シトシンがメチル化され、いわゆる第五の塩基として重要な生命情報を担うことが知られるが、こうした修飾は「エピゲノム」の重要な因子である。ロングリードシーケンスでは、メチル化されたシトシンも含めて、まるごと読み取れるようになっているという。
横浜市立大学では2019年に「神経核内封入体病」と呼ばれる、60歳前後に認知症を呈する疾患の遺伝子をロングリードシーケンサーで特定することに成功している。「GGC」という3塩基の配列が繰り返すもので、従来の解析手法では全く捉えることができなかった。
図・横浜市立大学で2019年に発足したメディカルゲノムセンター(出典:横浜市立大学)
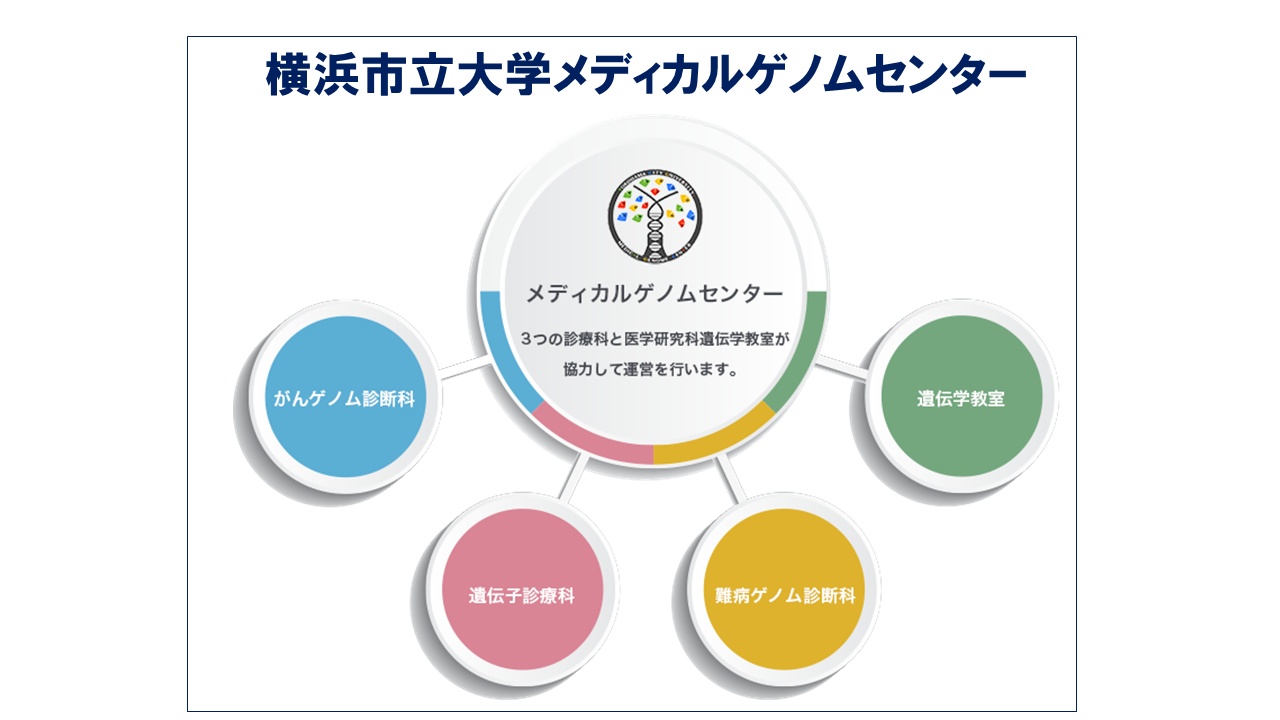
各部門が協力して難病やがんの遺伝子/ゲノム診断に対応している。
「気軽に連絡をしてほしい」
診断のつかない症例の遺伝子解析を検討する場合にはどうしたらよいのだろうか。
松本先生は、「各大学病院には遺伝子診療部ができてきています。そういうところを利用できます。分からない症状/疾患をそのままにするのではなく、その原因を探すことは重要です」と述べる。横浜市立大学附属病院では2019年からメディカルゲノムセンターが発足した。このセンターには難病ゲノム診断科・遺伝子診断科・がんゲノム診断科に加え我々の遺伝学教室が協力する体制で、難病やがんの遺伝子/ゲノム診断を進めており(参照:メディカルゲノムセンターのミッション)、こちらを利用が可能である。さらに、「希少難病は、基本極めてまれで患者はどこでどんな病院を受診するのか等の把握は難しい。システマティックなルートを作るのも重要ですが、医師からダイレクトに連絡を受けることも少なくありません。小児の難治てんかんなどは昭和大学小児科の加藤光広先生と連携して検体を送ってもらうルートもあります。積極的に応じて、検体を受け付けるスタイルは重要です」と松本先生は話す。
図・未診断疾患イニシアチブ(Initiative on Rare and Undiagnosed Diseases : IRUD、アイラド)のネットワーク(出典:日本医療研究開発機構=AMED)
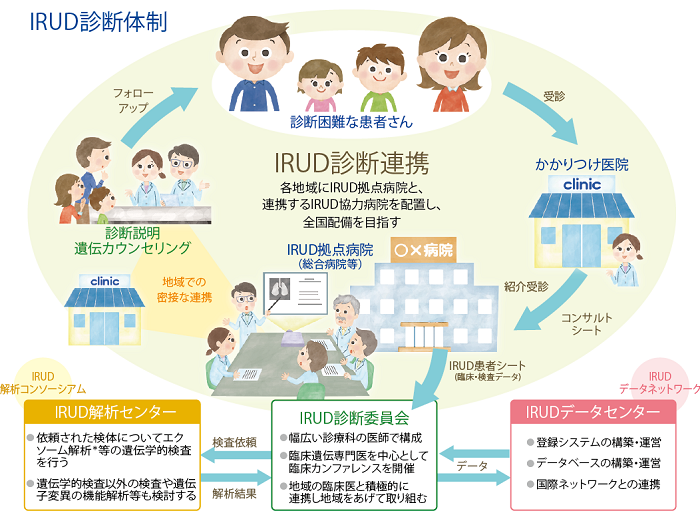
一方で、IRUDのネットワークを利用する方法もある。IRUDへの参加基準は、「2つ以上の臓器にまたがり、一元的に説明できない他覚的所見を有すること」または「何らかの遺伝子異常が疑われる病状であること(血縁者、兄弟に同じような病状が認められる場合を含む)」のいずれかの条件を満たすこと。その上で、「6カ月以上にわたって(乳幼児は除く)持続し、生活に支障のある症状があり、診断がついていない状態」としている。IRUDのプロジェクトでもこれまでに1308家系の遺伝子解析を行い、診断率が43%となった。36の新規疾患を見いだしている。
松本先生は、「将来的には治らなかった病気に対して積極的な治療ができる可能性は十分あります。診断ができなかった患者さんの原因が判明し、その未来が少しでも明るくなるために備えておくことも極めて重要なのです」と話す。
松本 直通(まつもと なおみち)先生
横浜市立大学大学院医学研究科遺伝学教室教授。1986年九州大学医学部卒業。九州大学産婦人科などでの勤務、長崎大学大学院医歯薬学総合研究科博士課程を経て、1997年シカゴ大学留学。2000年、長崎大学大学院医歯薬学総合研究科助教授。2003年より現職。
- 本ページでは、配信元であるステラ・メディックスが作成したコンテンツを医学および薬学の発展のために提供しております。本コンテンツは、弊社医薬品の広告宣伝を目的としたものではありません。


